- Tổng quan
- 1. Nguyên liệu và phương pháp
- 2. Kết quả và thảo luận
- 2.1. Ảnh hưởng của điều kiện gia nhiệt đến hàm lượng Sulforaphane của bột bông cải xanh khô đông lạnh
- 2.2. Ảnh hưởng của pH đến hàm lượng Sulforaphane trong huyền phù bông cải xanh trong nước và bột bông cải xanh khô đông lạnh
- 2.3. Ảnh hưởng của pH, bổ sung dầu và làm khô đông lạnh lên hàm lượng Sulforaphane
- 2.4. Ảnh hưởng của việc bảo quản đối với hàm lượng Sulforaphane của bột bông cải xanh khô đông lạnh và (dầu bông cải xanh)
- 3. Kết luận
- 4. Các chủ đề liên quan
- 5. Tham vấn chuyên môn
Hợp chất Sulforaphane: Hàm lượng Sulforaphane sẽ khác biệt như thế nào khi chế biến bằng những phương pháp khác nhau? Bổ sung dầu có phải là giải pháp?
Tổng quan
Người ta quan tâm đáng kể đến việc phát triển các thành phần làm từ bông cải xanh có chứa hàm lượng Sulforaphane cao vì hoạt chất này có khả năng làm giảm nguy cơ mắc một số bệnh. Glucoraphanin trong bông cải xanh được myrosinase chuyển thành Sulforaphane khi mô thực vật bị phá vỡ. Tính không ổn định của Sulforaphane ở nhiệt độ cao và trong môi trường nước tạo ra những thách thức cho việc phát triển các thành phần chứa hợp chất Sulforaphane. Sự thay đổi trong điều kiện xử lý nhiệt của huyền phù bông cải xanh, độ pH, bổ sung dầu và điều kiện bảo quản ảnh hưởng đến mức độ Sulforaphane.
Hàm lượng Sulforaphane của huyền phù bông cải xanh trong nước là hàm của pH (pH 4,0, 5,0 và 6,0) sau khi xử lý nhiệt (60 ° C / 5 phút) và giữ trong 4 giờ ở 25 ° C. Độ pH bằng 5 là tối ưu để sản xuất Sulforaphane. Việc thêm dầu vào huyền phù bông cải xanh trước khi làm khô đông lạnh sẽ làm chậm tốc độ phân hủy Sulforaphane trong quá trình bảo quản bột. Có rất ít sự khác biệt giữa tốc độ phân hủy của Sulforaphane trong bột (dầu bông cải xanh) làm từ nhũ tương pH 5 hoặc pH 6 (dầu bông cải xanh). Có những trở ngại đáng kể đối với việc phát triển bột bông cải xanh có hàm lượng Sulforaphane cao để sử dụng làm thành phần thực phẩm chức năng hoặc chất bổ sung.
1. Nguyên liệu và phương pháp
1.1. Nguyên liệu

Bông cải xanh (Brassica oleracea, var. Aurora) được lấy từ một nông trại địa phương (Fresh Select, Werribee South). Dầu cá ngừ có nguồn gốc từ NuMega Thành phần Pty Ltd (VIC, Úc). Tiêu chuẩn Sulforaphane là của Sigma-Aldrich Inc. (MO, Hoa Kỳ). Tiêu chuẩn này được sử dụng để tạo dung dịch chuẩn (gốc) 1 mg / mL với 30% (v / v) acetonitril, được bảo quản ở -18 ° C sau khi chuẩn bị. Axit fomic được lấy từ Ajax Finechem (Auckland, New Zealand). Acetonitril, etyl axetat và hexan thuộc HPLC loại, và etanol (≥99,5%) là loại phân tích (Tất cả các dung môi đều từ Merck, Darmstadt, Đức).
1.2. Sản xuất Sulforaphane trong các điều kiện khác nhau
1.2.1. Ảnh hưởng của nhiệt độ và điều kiện gia nhiệt
Ba thí nghiệm gia nhiệt đã được thực hiện:
- Thử nghiệm 1: Nước (1,24 kg) được làm nóng đến 65 hoặc 70°C trong bộ xử lý thực phẩm dùng trong nồi (Tefal Cuisine Companion, FE800A60, có gắn lưỡi dao C). Bông cải xanh (621 g) rửa sạch, cắt thành bông nhỏ (2 cm) cho vào nước nóng và ngâm ở tốc độ 9. Nhiệt độ được duy trì ở 65°C trong 30 phút hoặc 70°C trong 5 phút trong khi ngâm. Phần nước macerate được tiếp tục xử lý bằng máy xay cầm tay (Breville) ở tốc độ thấp trong 5 phút, tiếp theo là cắt bằng máy trộn cắt cao (máy trộn Silverson L4R) ở tốc độ 7 trong 10 phút để tạo ra hỗn hợp nhuyễn mịn (chứa 3,4% chất rắn). Bột nhuyễn được đông lạnh trong tủ đông -20°C và sau đó được làm khô bằng máy sấy đông lạnh quy mô phòng thí nghiệm. Bột khô được nghiền bằng máy xay cà phê và được sàng bằng sàng (cỡ sàng 300 μm) và được bảo quản ở 4°C cho đến khi phân tích. Để đối chứng, bông cải xanh thô được sấy khô đông lạnh mà không qua xử lý nhiệt.
- Thử nghiệm 2: Toàn bộ đầu bông cải xanh được rửa sạch và đun nóng trong lò hấp. Lò đã được làm nóng trước đến 70°C, và đặt bông cải xanh vào lò. Nhiệt độ lõi sản phẩm được theo dõi bằng đầu dò nhiệt độ. Khi nhiệt độ lõi bông cải xanh đạt 55, 60 hoặc 65°C (cho mỗi lần lặp lại tương ứng), nhiệt độ lõi của sản phẩm trong 6 phút cuối cùng của quá trình xử lý được ghi lại. Nhiệt độ lõi dao động từ 68 đến 75°C, 69–79°C và 68–87°C trong 6 phút cuối cùng của các nghiệm thức tương ứng. Mẫu được lấy ra khỏi tủ sấy và ngâm trong nước đá để làm nguội nhanh. Dùng khăn giấy lau sạch nước thừa từ bông cải xanh. Bông cải xanh đã được làm nóng được nghiền với nước (để thu được 8,1% chất rắn bông cải xanh) trong một máy xử lý thực phẩm trong nồi (Tefal Cuisine Companion, FE800A60, có gắn lưỡi dao C) ở tốc độ 9. Bột nhuyễn sau đó được đông lạnh trong tủ đông −20°C qua đêm và đông khô trong máy sấy đông quy mô phòng thí nghiệm. Bột khô đông lạnh được nghiền bằng máy xay cà phê và sàng sử dụng cỡ sàng 300 μm và được bảo quản ở 4°C cho đến khi phân tích. Để đối chứng, bông cải xanh thô và bông vụn đã được đông khô, xay, sàng bằng sàng 300 μm và được bảo quản ở 4°C cho đến khi phân tích.
- Thử nghiệm 3: Rửa sạch cả đầu bông cải xanh và cắt thành từng khoanh. Lò hơi đã được làm nóng trước đến 90°C. Bông cải xanh được đặt vào lò và nhiệt độ lõi sản phẩm được theo dõi bằng đầu dò nhiệt độ. Bông cải xanh được lấy ra khỏi lò sau khi nhiệt độ lõi bông cải xanh đạt ~ 85°C và duy trì trong 2 phút. Sau đó, bông cải xanh được ngâm trong nước đá. Nước thừa được loại bỏ bằng khăn giấy. Nước được thêm vào bông cải xanh và hỗn hợp được xay nhuyễn bằng máy xay nhà bếp (Optimum 9400, Optimum Appliance Pty. Ltd, VIC, Australia). Xay nhuyễn bông cải xanh được giữ ở 25°C trong 4 giờ, sau đó được làm đông lạnh ở -20°C trước khi làm khô đông lạnh trong máy sấy đông quy mô phòng thí nghiệm.
1.2.2. Ảnh hưởng của pH và bổ sung dầu
Ba thử nghiệm riêng biệt, gọi là Thử nghiệm 4, Thử nghiệm 5 và Thử nghiệm 6, đã được thực hiện, mỗi thử nghiệm có một nguồn bông cải xanh tươi (Hình 1). Tóm lại, đầu bông cải xanh được cắt thành các phần tư được nung ở nhiệt độ 60°C trong 5 phút. Dung dịch nước được giữ trong 4 giờ ở ~ 25°C, sau đó được làm đông lạnh trong tủ đông -20°C qua đêm trước khi làm khô đông lạnh. Trong Thử nghiệm 4, huyền phù bông cải xanh được tạo ra ở pH tự nhiên (pH ~ 6,0). Trong Thử nghiệm 5 & 6, độ pH của huyền phù bông cải xanh cũng được điều chỉnh thành pH 4,0 và pH 5,0 tương ứng ngoài pH tự nhiên.
Để điều chế nhũ tương (dầu bông cải xanh), dầu đã được thêm vào huyền phù bông cải xanh (Hình 1). Các mẫu đã chọn được làm đông lạnh ở -20°C và sau đó làm khô đông lạnh. Thông tin chi tiết được đưa ra bên dưới. Hỗn dịch bông cải xanh trong nước: Đối với những thí nghiệm này, đầu bông cải xanh tươi được cắt thành các phần tư được hấp (nhiệt độ lõi 60°C / 5 phút) trong lò hấp (Comcater Pty Ltd., VIC, Australia). Xử lý nhiệt S. Zhang, et al. LWT – Khoa học và Công nghệ Thực phẩm 128 (2020) được chọn vì có đủ hoạt động myrosinase còn lại trong những điều kiện này, nơi quá trình chuyển đổi thành nitrile bị giảm xuống do sự bất hoạt của protein epithiospecifier (Van Eylen et al., 2007).
Sau khi xử lý nhiệt, đầu bông cải xanh được cắt thành các phần tư được làm lạnh trên đá. Đá và nước dư thừa đã được rũ bỏ. Bông cải xanh được nghiền nhỏ và sau đó xay nhuyễn với nước thêm ở các độ pH khác nhau. Các huyền phù bông cải xanh trong nước (~ 5–7% w/w chất rắn bông cải xanh) ở pH tự nhiên (pH ~ 6) hoặc pH có tính axit (pH 4 và pH 5, được axit hóa với thể tích xác định trước là axit axetic 0,1 M) được giữ để 4 giờ ở 25°C để myrosinase hoạt động dựa trên glucoraphanin để chuyển đổi thành Sulforaphane. Những người khác đã chỉ ra rằng nhiệt độ 14–25°C là tối ưu cho sự hình thành Sulforaphane (Dosz và Jeffery, 2013).
Phần lớn huyền phù bông cải xanh trong nước được lấy mẫu nhỏ và sử dụng để xác định hàm lượng Sulforaphane. Một phần huyền phù bông cải xanh còn lại được đông lạnh trong tủ đông -20°C qua đêm và sau đó làm khô đông lạnh trong máy sấy đông quy mô phòng thí nghiệm. Một phần khác được làm lạnh đến 4°C và sau đó được vận chuyển đến cơ sở thương mại để làm khô đông lạnh, nơi nó đã được làm đông lạnh trước khi làm khô đông lạnh.
(Dầu bông cải xanh) trong nhũ tương nước: Để điều chế (dầu bông cải xanh) ở dạng nhũ tương nước (thành phần mục tiêu ~ 5% w / w chất rắn bông cải xanh và ~ 5% w / w dầu cá ngừ), dầu cá ngừ đã được trộn với huyền phù nước để tạo thành tiền nhũ tương, sau đó được đồng nhất bằng cách sử dụng UltraTurrax (Crown Scientific Industries Inc., NSW, Australia) hoạt động ở tốc độ 13.500 vòng / phút trong 1 phút. Các mẫu được làm đông lạnh ở -20°C và làm khô đông lạnh trong máy sấy đông lạnh quy mô phòng thí nghiệm hoặc làm lạnh đến 4°C trước khi vận chuyển đến cơ sở thương mại để làm khô đông lạnh. Sấy đông lạnh: Để làm khô đông lạnh tại CSIRO, huyền phù và nhũ tương ở pH chưa điều chỉnh, được đông lạnh trong khay ở -20°C sau khi chuẩn bị và các mẫu đông lạnh được làm khô đông lạnh trong máy sấy đông quy mô phòng thí nghiệm (Máy sấy đông lạnh Dynavac, Mẫu FD-5 , Dynapump, Úc).
Đối với Thử nghiệm 6, một phần mẫu được đông lạnh ở -20°C và sau đó được làm khô đông lạnh tại CSIRO. Các phần còn lại được ướp lạnh qua đêm (ở nhiệt độ 4°C) sau đó được vận chuyển đến cơ sở thương mại để làm khô đông lạnh. Bột được bảo quản trong túi nhựa đen ở -18°C, 4°C và 25°C và được phân tích theo khoảng thời gian trong quá trình bảo quản.

Hình 1. Chuẩn bị huyền phù bông cải xanh trong nước, nhũ tương (dầu bông cải xanh) và bột đông khô
1.3. Quy trình chiết xuất và định lượng Sulforaphane
Hàm lượng Sulforaphane của huyền phù bông cải xanh trong nước và (dầu bông cải xanh) được xác định trong vòng một ngày kể từ khi chuẩn bị, nơi mẫu được bảo quản ở 4°C trước khi phân tích. Bột đã được lấy ra khỏi kho và phân tích trong vòng một ngày.
1.3.1. Chiết xuất Sulforaphane từ bột bông cải xanh có và không có dầu
Ethyl acetate được sử dụng để chiết Sulforaphane từ huyền phù bông cải xanh trong nước và đông lạnh bột bông cải xanh khô không dầu (Li và cộng sự, 2012). Huyền phù bông cải xanh trong nước (5g) hoặc bột bông cải xanh (0,25g) được chiết bằng 15 ml etyl axetat. Các mẫu được quay xoáy trong một phút, ngâm trong 5 phút và sau đó lắc trong một giờ ở nhiệt độ phòng (22°C) trên máy lắc nằm ngang (Ratek Instruments Pty. Ltd., VIC, Australia).
Sau đó, các mẫu được ly tâm ở 5000g trong 20 phút ở 10°C và các chất nổi phía trên được thu thập. Quá trình chiết được lặp lại hai lần đối với bột hoặc ba lần đối với huyền phù trong nước. Các chất nổi phía trên từ tất cả các phần chiết xuất được gộp lại, cho mỗi mẫu và được làm bay hơi bằng Máy cô đặc chân không SpeedVac (Thermo Fisher Scientific Inc., CA, Hoa Kỳ). Các chất chiết khô được hòa tan trong acetonitril 30% (v / v) bằng cách xoáy trong 1 phút và ngâm trong 5 phút. Các dung dịch được lọc qua màng lọc 0,22 μm trước khi phân tích Sulforaphane trên UPLC. Đối với bột có chứa dầu, hỗn hợp etyl axetat-hexan 1: 4 hoặc 1: 1 được sử dụng để chiết xuất Sulforaphane và người ta thấy rằng hỗn hợp 1: 1 có độ thu hồi Sulforaphane cao hơn.
Tóm lại, Sulforaphane được chiết xuất từ các mẫu bằng cách sử dụng hỗn hợp etyl axetat-hexan như đã mô tả ở trên. Sau đó, tách chiết pha rắn (SPE) được thực hiện để loại bỏ dầu và tinh chế dịch chiết thô. Phần chiết khô còn lại sau khi làm bay hơi dung môi được hòa tan trong 1,5 mL etyl axetathexan bằng cách xoáy trong 1 phút và ngâm trong 5 phút. Các dung dịch được nạp vào cột SPE (cột silica 55 μm × 70 Å trong ống 3 mL, Phenomenex Inc., CA, USA) trước đó đã được điều hòa bằng hexan. Sau đó, các cột được rửa bằng 1,2 mL ethyl (Hình 1). Chuẩn bị huyền phù bông cải xanh trong nước, nhũ tương (dầu bông cải xanh) và bột khô đông lạnh. S. Zhang và cộng sự. LWT – Khoa học và Công nghệ Thực phẩm 128 (2020) axetat và Sulforaphane được rửa giải bằng 3 mL etanol.
Quá trình nạp mẫu, rửa cột và rửa giải được tiến hành trong điều kiện chân không. Các chất rửa giải được làm khô trong Máy cô đặc chân không SpeedVac để loại bỏ etanol. Các cặn khô sau đó được hòa tan trong 2,0 mL acetonitril 30% (v / v) và phân tích Sulforaphane như mô tả ở trên. Trong thí nghiệm sơ bộ, sự thu hồi của cột Sulforaphane được kiểm tra bằng cách cho một lượng Sulforaphane đã biết vào dầu, sau đó được hòa tan trong ethyl acetate-hexane (1: 4) và được nạp vào cột SPE. Sự thu hồi được tìm thấy là 94% khi hỗn hợp etyl axetat-hexan (1: 4) được sử dụng để chiết xuất Sulforaphane. Độ thu hồi cao hơn một chút thu được khi sử dụng axetat-hexan (1: 1). Do đó, các giá trị thu được từ dữ liệu UPLC cho các mẫu chứa dầu đã được điều chỉnh bằng hệ số thu hồi.
1.3.2. Định lượng Sulforaphane
Nồng độ Sulforaphane được xác định bằng cách sử dụng hệ thống Acquity ™ Ultra Performance LC (Waters Corporation, Milford, MA, USA), được trang bị bộ quản lý phân phối dung môi nhị phân và bộ quản lý mẫu. Sự phân tách sắc ký được thực hiện trên cột sắc ký Acquity BEH C18, 2,1 × 50 mm. Pha động, A và B, bao gồm 0,1% axit fomic trong nước Milli-Q và 0,1% axit fomic trong axetonitril. Phân tích được thực hiện với tốc độ dòng chảy 0,35 mL / phút với tổng thời gian chạy là 8 phút. Nhiệt độ cột được giữ không đổi ở 30°C.
Hợp chất Sulforaphane được phát hiện ở bước sóng 205 nm với đỉnh xuất hiện ở ~ 1,35 phút. Phân tích quang phổ của đỉnh này đã xác nhận danh tính của Sulforaphane. Để định lượng Sulforaphane, đường chuẩn của lượng Sulforaphane (μg) so với diện tích pic Sulforaphane được xây dựng. Dung dịch làm việc Sulforaphane ở nồng độ 0,1 mg / mL trong axetonitril 30% được chuẩn bị mới từ dung dịch gốc (1 mg / mL trong axetonitril 30%) để xây dựng đường chuẩn. Hàm lượng Sulforaphane của tất cả các loại bột (có và không có dầu) được biểu thị bằng μMol / g chất rắn bông cải xanh.
1.4. Phân tích thống kê
Dữ liệu được phân tích bằng cách sử dụng phân tích phương sai (ANOVA) trên trang web VassarStats (http://vassarstats.net/). Thử nghiệm này xác định xem có sự khác biệt giữa các mẫu hay không. Xác suất p <0,05 được coi là có ý nghĩa thống kê.
2. Kết quả và thảo luận
2.1. Ảnh hưởng của điều kiện gia nhiệt đến hàm lượng Sulforaphane của bột bông cải xanh khô đông lạnh
Ảnh hưởng của các điều kiện gia nhiệt khác nhau đến mức độ Sulforaphane trong bột làm từ bông cải xanh đã được đun nóng, đông lạnh và sấy khô được cho trong Bảng 1. Có một lượng Sulforaphane thấp trong bông cải xanh khô đông lạnh chưa được đun nóng trước đó trong nước (0,19 μMol / g chất rắn bông cải xanh, Thử nghiệm 1), nhưng xử lý nhiệt trong nước ở 65°C trong 30 phút hoặc 70°C trong 5 phút trước khi sấy đông lạnh làm tăng hàm lượng Sulforaphane (0,96–1,10 μMol / g chất rắn bông cải xanh, Thử nghiệm 1). Những nghiên cứu khác đã báo cáo rằng bông cải xanh chưa nấu chín có 16,64 μg Sulforaphane/ g DW (tức là ~ 0,1 μMol / g DW), thấp hơn một chút so với mức 0,19 μMol / g chất rắn bông cải xanh trong các thử nghiệm của chúng tôi (Bảng 1).
Đối với Thử nghiệm 1 & 2, tùy thuộc vào quá trình xử lý nhiệt và lô bông cải xanh được sử dụng, mức thu được sau khi làm khô đông lạnh là từ 0,96 đến 1,96 μMol / g chất rắn bông cải xanh (Bảng 1). Ngoại lệ là Thử nghiệm 3 trong đó có Sulforaphane không đáng kể (<0,01 μMol / g chất rắn bông cải xanh), nhưng kết quả này một phần có thể liên quan đến nhiệt độ lò cao hơn (90°C) trong Thử nghiệm 3 trước khi nhiệt độ lõi sản phẩm đạt 85°C. Hoạt động của myrosinase bị giới hạn ở nhiệt độ trên 80°C (Bjorkman & Lonnerdal, 1973).
Người ta đã báo cáo rằng 90% hoạt tính của myrosinase bị mất sau 10 phút ở 60°C do sự bất hoạt của enzyme (Van Eylen et al., 2007). Tuy nhiên, nhiệt độ tăng cũng làm tăng tốc độ chuyển glucoraphanin thành Sulforaphane. Do đó có những tác động ngược lại do tăng tốc độ chuyển đổi và giảm hoạt động của enzym sẽ ảnh hưởng đến mức Sulforaphane. Những người khác báo cáo rằng không có Sulforaphane có thể phát hiện được khi đun sôi (20 phút) hoặc cho vào lò vi sóng (19 phút) hoặc hấp (Tabart và cộng sự, 2018). Tuy nhiên, việc ủ bông cải xanh đông lạnh trong lò vi sóng (theo hướng dẫn của nhà sản xuất) sau đó để thời gian thủy phân 20 phút hoặc 24 giờ và làm khô đông lạnh dẫn đến hàm lượng Sulforaphane <0,42–2,55 μmol / g DW (Dosz và Jeffery, 2013). Pérez, Barrientos, Román và Mahn (2014) cho rằng điều kiện chần tối ưu để sản xuất Sulforaphane là ngâm trong nước ở 57°C trong 13 phút. Trong các thí nghiệm của họ khi ngâm bông cải xanh (300 g) trong nước (1,5 L nước) trong bể điều nhiệt, đã thu được giá trị ~ 4 μmol / g DW (Pérez và cộng sự, 2014).
Nhìn chung, các kết quả thử nghiệm của chúng tôi và các kết quả trong tài liệu cho thấy rằng ngay cả những thay đổi nhỏ trong điều kiện xử lý nhiệt và tải nhiệt mà các mẫu phải trải qua cũng có thể ảnh hưởng đến mức Sulforaphane thu được. Điều này cho thấy thực tế là có những thách thức đáng kể trong việc kiểm soát quá trình gia nhiệt để đạt được mức Sulforaphane mục tiêu trong bột bông cải xanh. Ngoài ra còn có ảnh hưởng của giống, mùa vụ, điều kiện nông học và các yếu tố sau thu hoạch sẽ ảnh hưởng đến mức glucoraphanin, hoạt động myrosinase và do đó là mức Sulforaphane có thể thu được. Ví dụ, xử lý melatonin ảnh hưởng đến mức glucoraphanin và Sulforaphane trong bông cải xanh cắt tươi sau khi thu hoạch (Wei, Liu, Zheng, & Zheng, 2020).
Bảng 1
Ảnh hưởng của điều kiện gia nhiệt tiếp theo là làm khô đông lạnh đến hàm lượng Sulforaphane của bột bông cải xanh đông khô (không có dầu).
| Mẫu | Điều kiện nhiệt độ-thời gian xử lý | Sulforaphane (μMol/g chất rắn bông cải xanh) |
| THỬ NGHIỆM 1: Xử lý nhiệt trong nước | ||
| Bông cải xanh (2 cm) | không xử lý nhiệt | 0,19 |
| Bông cải xanh (2 cm) | 65 ° C trong 30 phút | 0,96 |
| Bông cải xanh (2 cm) | 70 ° C trong 5 phút | 1.10 |
| THỬ NGHIỆM 2: Xử lý nhiệt trong lò hấp (làm nóng trước đến 70 ° C) | ||
| Đầu bông cải xanh (cắt nhỏ) | không xử lý nhiệt | 1.89 |
| Đầu bông cải xanh (toàn bộ) | Nhiệt độ lõi 68–75 ° C trong 6 phút | 1,66 |
| Đầu bông cải xanh (toàn bộ) | Nhiệt độ lõi 69–79 ° C trong 6 phút | 1,96 |
| Đầu bông cải xanh (toàn bộ) | Nhiệt độ lõi 68–87 ° C trong 6 phút | 1,50 |
| THỬ NGHIỆM 3: Xử lý nhiệt trong lò hấp (làm nóng trước đến 75–80 ° C) | ||
| Đầu bông cải xanh (phần tư) | Nhiệt độ lõi 85 ° C trong 2 phút | <0,01 |
Thử nghiệm 2: Nhiệt độ lò được giữ ở 70°C. Khi nhiệt độ lõi của mẫu đạt 55, 60 hoặc 65°C, lò sẽ tắt sau 9 phút và nhiệt độ lõi sản phẩm được ghi lại trong 6 phút qua.
Thử nghiệm 3: Nhiệt độ tủ sấy giữ ở 90°C, khi nhiệt độ lõi của mẫu đạt 85°C.
2.2. Ảnh hưởng của pH đến hàm lượng Sulforaphane trong huyền phù bông cải xanh trong nước và bột bông cải xanh khô đông lạnh
Bảng 2 cho thấy ảnh hưởng của độ pH tại thời điểm ngâm nước, tiếp theo là giữ trong 4 giờ ở 25°C đối với hàm lượng Sulforaphane của huyền phù bông cải xanh trong nước và bột bông cải xanh. Mặc dù có sự khác biệt đáng kể về lượng Sulforaphane tuyệt đối đo được trong các thử nghiệm khác nhau, có những xu hướng đang xuất hiện từ dữ liệu thu được. Hàm lượng Sulforaphane cao nhất thu được ở pH 5 cho cả hỗn dịch nước và bột đông khô (Bảng 2).
Những kết quả này phù hợp với Dosz và Jeffery (2013), những người đã báo cáo rằng pH 5 là tối ưu để sản xuất Sulforaphane và không có sự khác biệt đáng kể giữa việc tạo Sulforaphane giữa pH 5 và 6 nhưng sản xuất Sulforaphane ở pH 4 thấp hơn đáng kể so với ở pH càng cao. Tuy nhiên, những người khác đã kiểm tra hàm lượng Sulforaphane như một hàm của độ pH và nhiệt độ của một loạt các loại rau họ cải cho thấy rằng sự hình thành isothiocyanate tăng lên ở độ axit (pH 4) hoặc pH cơ bản (pH 8) ở nhiệt độ từ 4 đến 37 ° C (Hanschen et al., 2018), có thể do Sulforaphane ổn định hơn ở pH axit (Wu, Mao, You, & Liu, 2014). Sulforaphane không ổn định trong môi trường nước cũng như trong dung môi protic (Franklin và cộng sự, 2014).
Ngoài ra, trong các nghiên cứu của mình, chúng tôi đã sử dụng axit axetic, một dung môi protic phân cực, để điều chỉnh độ pH về độ pH 4 vì nó là một axit thực phẩm thông thường. Điều này có thể đã góp phần làm giảm hàm lượng Sulforaphane trong hệ thống pH 4 (Bảng 2), mặc dù Sulforaphane ổn định hơn ở pH thấp (Wu và cộng sự, 2014).
Bảng 2: Hàm lượng Sulforaphane của huyền phù bông cải xanh trong nước (5,5–7,0% TS) và bột bông cải xanh khô đông lạnh (không dầu).
| Mẫu | Sulforaphane (μMol / g chất rắn bông cải xanh) | |||
| pH 4 | pH 5 | pH 6 | ||
| Thử nghiệm 4 | Sự ngưng tụ | Chưa xong | Chưa xong | 2.71 |
| Bột | Chưa xong | Chưa xong | 0.42 | |
| Thử nghiệm 5 | Sự ngưng tụ | 0.08 | 1.82 | 0.16 |
| Bột | Chưa xong | Chưa xong | < 0.01 | |
| Thử nghiệm 6 | Sự ngưng tụ | 3.62 | 4.09 | 3.85 |
| Bột | 0.39 | 0.73 | 0.59 | |
* Ảnh hưởng của độ pH, xử lý sau xử lý và làm khô đông lạnh: * (Bông cải xanh đã được làm nóng ở 60 ° C trong 5 phút, huyền phù nước.
2.3. Ảnh hưởng của pH, bổ sung dầu và làm khô đông lạnh lên hàm lượng Sulforaphane
Ảnh hưởng của sấy đông lạnh lên hàm lượng Sulforaphane của bột được tạo ra từ huyền phù và nhũ tương bông cải xanh trong nước được đưa ra trong Hình 2. Đông lạnh bột khô được tạo ra từ huyền phù và nhũ tương trong nước được đông lạnh và sau đó làm khô đông lạnh đã làm giảm đáng kể mức độ Sulforaphane so với của cùng một mẫu trước khi làm khô đông lạnh. Chỉ có 11–25% lượng Sulforaphane ban đầu còn lại sau khi làm khô đông lạnh. Đây là một sự phân huỷ đáng kể của Sulforaphane. Kết quả của chúng tôi trái ngược với Dosz và Jeffery (2013), những người đã gợi ý rằng không có tổn thất nào khi làm khô đông lạnh huyền phù bông cải xanh trong các thí nghiệm trong phòng thí nghiệm. Sự khác biệt có thể là trong việc xử lý huyền phù trong quá trình sản xuất bột.
Trong các nghiên cứu của chúng tôi, các mẫu được đông lạnh trong khay (tức là đông lạnh chậm) khi bột được sản xuất tại cơ sở của chúng tôi để mô phỏng một phương pháp có thể được sử dụng thực tế trong công nghiệp. Cần lưu ý rằng hàm lượng Sulforaphane trong bột sản xuất tại cơ sở của chúng tôi khác với hỗn dịch và nhũ tương được làm lạnh và vận chuyển đến cơ sở bên ngoài để làm khô đông lạnh.
Ví dụ, trong Thử nghiệm 6, bột (dầu bông cải xanh) được sản xuất trong máy sấy đông lạnh quy mô phòng thí nghiệm có hàm lượng Sulforaphane là 0,71 μMol / g chất rắn bông cải xanh (Hình 2) trong khi bột được làm khô tại cơ sở thương mại có hàm lượng Sulforaphane là 0,96 μMol / g chất rắn bông cải xanh. Điều này cho thấy rằng các điều kiện xử lý bao gồm bảo quản và vận chuyển lạnh hỗn dịch / nhũ tương bao gồm vận chuyển bột giữa các cơ sở có thể có tác động đến hàm lượng Sulforaphane. Khi myrosinase vẫn còn hoạt động, có thể sẽ có một số thế hệ Sulforaphane, đặc biệt là trong quá trình xử lý.
Những nghiên cứu khác đã chỉ ra rằng có thể hình thành Sulforaphane trong quá trình làm khô khay (Mahn, Martin, Reyes, & Saavedra, 2016). Do đó, lượng Sulforaphane quan sát được do đó sẽ bị ảnh hưởng bởi tốc độ hình thành Sulforaphane và tốc độ phân hủy Sulforaphane xảy ra đồng thời. Có ý kiến cho rằng cần giảm thiểu việc tiếp xúc với nhiệt độ cao trong quá trình xử lý và bảo quản các sản phẩm có chứa Sulforaphane, cả ở trạng thái ướt và dạng bột để cải thiện tính nhất quán của các thành phần chứa Sulforaphane được làm từ nguyên liệu thực vật.
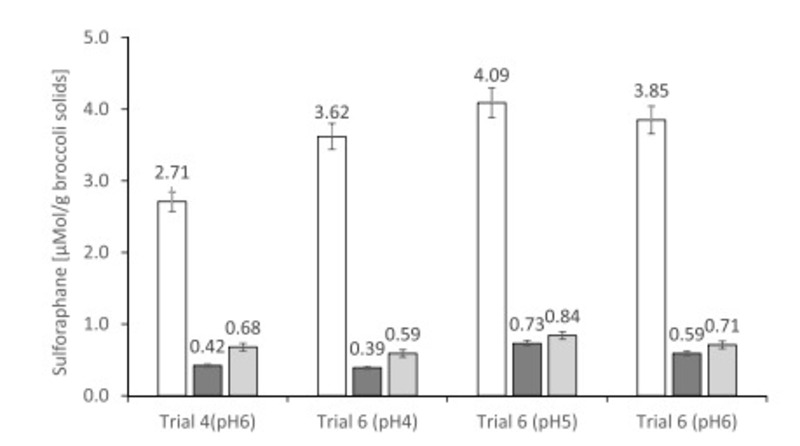
Hình 2. Ảnh hưởng của quá trình đông khô lên hàm lượng Sulforaphane trong huyền phù bông cải xanh trong nước và đông lạnh bột bông cải xanh khô có hoặc không có dầu (bông cải xanh được làm nóng ở 60 ° C trong 5 phút, huyền phù nước được giữ trong 4 giờ ở ~ 25 ° C sau đó đông khô, Thử nghiệm 4 & 6). Tất cả các loại bột đều được sản xuất trong một máy sấy đông lạnh quy mô phòng thí nghiệm. Chú giải: Thanh không đầy – Dịch huyền phù; Thanh điền đen: Bột bông cải xanh; Thanh màu xám: (Dầu bông cải xanh).
2.4. Ảnh hưởng của việc bảo quản đối với hàm lượng Sulforaphane của bột bông cải xanh khô đông lạnh và (dầu bông cải xanh)
Ảnh hưởng của việc bảo quản đối với hàm lượng Sulforaphane của bột bông cải xanh khô đông lạnh và bột bông cải xanh khô đông lạnh (dầu bông cải xanh) được thể hiện trong Hình. 3 và 4.
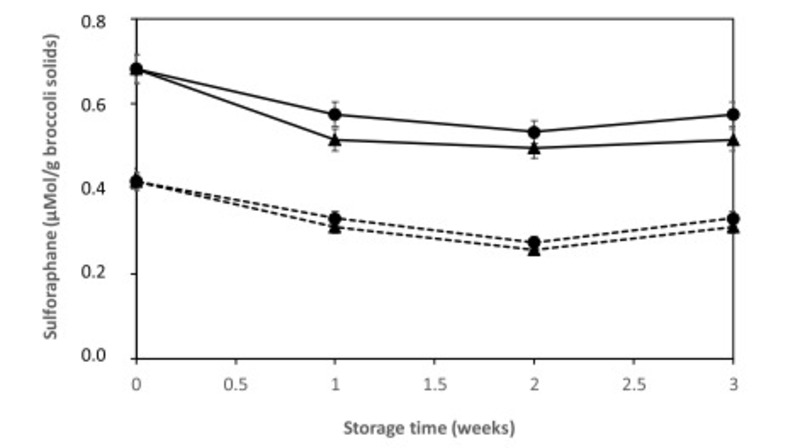
Hình 3. Ảnh hưởng của việc bảo quản đến hàm lượng Sulforaphane của bột bông cải xanh khô đông lạnh (độ ẩm 7%) và (dầu bông cải xanh) (độ ẩm 10%). Dữ liệu từ Thử nghiệm 4 (pH 6). Bột được sản xuất trong một máy sấy đông lạnh quy mô phòng thí nghiệm. Chú giải: Vạch chấm với điểm đánh dấu tròn – bột bông cải xanh được bảo quản ở -18 ° C; Vạch chấm bằng bút đánh dấu tam giác – bột bông cải xanh bảo quản ở 4 ° C; Vạch liền với điểm đánh dấu tròn – bột (dầu súp lơ xanh) được bảo quản ở -18 ° C; Vạch liền với điểm đánh dấu tam giác – bột (dầu súp lơ xanh) được bảo quản ở 4 ° C.
Trong bột làm từ cùng một mẫu bông cải xanh trong một cuộc thử nghiệm, lượng Sulforaphane tuyệt đối trong bột (dầu bông cải xanh) cao hơn so với bột bông cải xanh không thêm dầu (Hình 3). Mặc dù hàm lượng Sulforaphane ban đầu tuyệt đối khác nhau đối với các loại bột được chế biến vào những dịp khác nhau, hàm lượng Sulforaphane của tất cả các loại bột đều giảm khi bảo quản và có nhiều Sulforaphane được bảo quản ở 4°C và -18°C hơn ở 25°C (Hình 3 và 4).
Đáng chú ý, tốc độ phân hủy của Sulforaphane trong tất cả các loại bột không khác biệt rõ rệt khi các loại bột này được bảo quản ở -18°C hoặc 4°C (Hình 3 và 4). Có rất ít sự khác biệt giữa tốc độ phân giải Sulforaphane trong bột (dầu bông cải xanh) làm từ nhũ tương pH 5 hoặc pH 6 (dầu bông cải xanh) trong một thử nghiệm, mặc dù hàm lượng tuyệt đối của Sulforaphane là khác nhau (dữ liệu không được hiển thị). Không có dữ liệu so sánh từ các tài liệu về độ ổn định của Sulforaphane trong bột (dầu súp lơ xanh-cá ngừ). Tuy nhiên, các xu hướng quan sát được song song với những xu hướng quan sát được về sự ổn định của Sulforaphane trong nhũ tương kem bôi tại chỗ. Mặc dù chất nền khác với chất nền được sử dụng trong nghiên cứu của chúng tôi, sự phân hủy Sulforaphane được chứng minh là tăng ở nhiệt độ cao hơn nhưng việc bổ sung một pha hữu cơ làm giảm tốc độ phân hủy Sulforaphane trong nhũ tương kem bôi tại chỗ giữa pH 5 và pH 6 (Franklin và cộng sự, 2014).
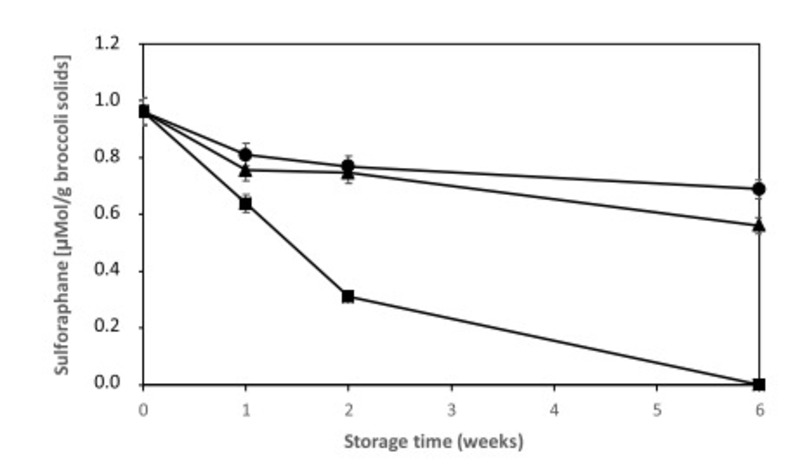
Hình 4. Ảnh hưởng của việc bảo quản ở -18 °C, 4 °C và 25 °C đến hàm lượng Sulforaphane trong bột khô (dầu bông cải xanh) đông khô. Bột từ Thử nghiệm 6 (pH6) được sản xuất trong một máy sấy đông lạnh thương mại. Chú giải: Vạch liền với điểm đánh dấu tròn – bột (broccolioil) được bảo quản ở -18 °C; Vạch liền với điểm đánh dấu tam giác – bột (dầu súp lơ xanh) được bảo quản ở 4 °C; Vạch liền với bút dạ vuông – bột (dầu súp lơ xanh) được bảo quản ở 25 °C.
3. Kết luận
Các nghiên cứu của chúng tôi đã chứng minh sự khác biệt lớn về hàm lượng Sulforaphane của bông cải xanh đã qua chế biến, khi chúng được chế biến theo cùng một phương pháp. Ngoài sự khác biệt về nguyên liệu ban đầu, sự nhạy cảm của hàm lượng Sulforaphane với các điều kiện chế biến và xử lý cũng như tính dễ bị phân hủy của nó khiến cho việc sản xuất một sản phẩm có nguồn gốc thực vật với lượng Sulforaphane được nhắm mục tiêu trở nên khó khăn. Bổ sung dầu có thể là một chiến lược để cản trở sự phân hủy của hợp chất Sulforaphane. Tuy nhiên, cần có các nghiên cứu có hệ thống hơn nữa để nâng cao hiểu biết về các điểm kiểm soát quan trọng để cải thiện tính nhất quán của các sản phẩm Sulforaphane có nguồn gốc thực vật.
4. Các chủ đề liên quan
Dưới đây là một số bài viết về các chủ đề nghiên cứu có liên quan đến hoạt chất Sulforaphane và công dụng của chúng:
- Các nghiên cứu về các yếu tố ngoại sinh thúc đẩy hàm lượng Sulforaphane trong mầm bông cải xanh và ảnh hưởng của nó đối với dòng tế bào ung thư vú
- Tác dụng của Sulforaphane khi tập luyện sức đề kháng nặng
- Sulforaphane làm giảm căng thẳng oxy hóa và tình trạng viêm
5. Tham vấn chuyên môn
- Bác sĩ
- Nguồn tham khảo: https://www.sciencedirect.com/science/article/abs/pii/S0023643820304321

